|
Где можно посмотреть информацию о физических ограничениях на значения характеристик компьютеров |
Свойства молекул, лежащие в основе молекулярной элементной базы информатики
Молекулярное распознавание
Любое из описанных выше свойств молекул можно применить для кодирования, передачи, хранения и обработки информации. Но, наверное, исторически первым свойством молекул, которое было использовано природой уже миллиарды лет тому назад, еще на добиологической стадии химической эволюции на Земле, было свойство молекулярного распознавания (англ. – molecular recognition). Именно оно сделало возможными возникновение и последующую эволюцию катализаторов, – молекул и ансамблей молекул, значительно ускоряющих ход определенных химических реакций.
Свойство молекулярного распознавания широко используют и в новейшей информатике, в первую очередь – в сенсорике – технической науке о построении и использовании сенсоров.
Сенсор – это устройство (узел, прибор, орган), которое превращает физические (физико-химические) свойства объекта наблюдения и их изменения в информационный сигнал для пользователя.
Сенсоры – это именно те устройства, в которых "рождается" информация, являющаяся основой для разумного поведения, для формирования и совершенствования информационных моделей окружающего мира в "разумных" системах. Ведь любая разумная система независимо от того, возникла она естественным путем или создана искусственно, успешно функционирует и выживает в реальном мире лишь до тех пор, пока она получает объективную и качественную информацию об этом мире.
Люминесцентные молекулярные сенсоры
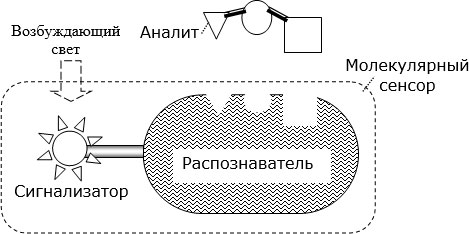
Молекулярные сенсоры очень распространены в живой природе. А вот первые искусственные сенсоры молекулярных размеров были созданы только в последние десятилетия ХХ в. Это – специально синтезированные макромолекулы, в состав которых входят два важных звена ( рис. 3.17). Одно из них является избирательно чувствительным к аналиту – молекулам того химического или биохимического вещества, наличие которого надо выявить и определить его концентрацию, – или к тем факторам внешней среды, которые надо контролировать. Это звено называют распознавателем (англ. recognition element). Часто для этого используют молекулы естественных биохимических ферментов (энзимов). Но используют и искусственно синтезированные распознаватели. Второе звено имеет выраженную люминесцентную активность, т.е. ярко светится под действием коротковолнового внешнего света или другого возбуждающего фактора. Это звено называют сигнализатор (англ. reporter).
В составе макромолекулы эти два звена взаимодействуют так, что, когда к распознавателю присоединяется частица искомого аналита или на него действует специфический внешний фактор, то это приводит к гашению или, наоборот, к стимулированию люминесценции сигнализатора.
Таким образом, описанный молекулярный сенсор, изменяя интенсивность люминесценции, сигнализирует о наличии и концентрации в окружающей среде молекул аналита или об изменении характеристик другого специфического внешнего фактора (например, температуры, кислотности среды и др.). Подчеркнем, что как полноценный сенсор самостоятельно действует каждая отдельная макромолекула!
Описанные молекулярные сенсоры называют "сенсорами с люминесцентным маркером". Будучи полноценным сенсором, но имея молекулярные размеры, они не рассчитаны на непосредственную работу с такими "пользователями", как человек или макроскопический прибор. Ведь интенсивность люминесценции отдельной молекулы относительно слаба, из-за чего ее тяжело заметить на фоне посторонних световых помех. Поэтому сейчас используют много (миллионы, миллиарды) одинаковых молекулярных сенсоров. Их общее люминесцентное излучение позволяет строить макроскопические сенсоры.
Например, синтезирован люминесцентный молекулярный сенсор для выявления присутствия в окружающей среде органофосфатов, входящих в состав инсектицидов и ряда нейротоксинов, вредных для здоровья человека. Звеном, селективно распознающим наличие органофосфатов, является в нем фермент органофосфатгидролаза (англ. organophosphate hydrolase – OPH), а сигнализатором – карбоксинафтофлуоресцеин (англ. carboxynaphtho-fluorescein – CNF). Используя чувствительный фотоприемник, удалось построить портативный сенсор, сообщающий о наличии органофосфатов уже при концентрациях от 50 нмоль/л. Количественное измерение концентрации, например, пароксона выполняется в диапазоне от 1 до 800 мкмоль/л.
Молекулярное распознавание на поверхности наночастиц металла
Для эффективного применения способности молекул к избирательному распознаванию были использованы также не известные прежде свойства наночастиц (далее – НЧ) металла размером порядка 1–600 нм. Как мы уже отмечали, электронная плазма таких НЧ способна колебаться с частотами до 1016 Гц. В зависимости от вида металла, от своих размеров и формы НЧ имеет свои характерные резонансные частоты колебаний электронной плазмы. Когда частота внешнего электромагнитного поля совпадает с резонансной, НЧ очень активно взаимодействуют с таким полем. НЧ таких металлов, как золото и серебро, на резонансных частотах рассеивают и поглощают свет намного сильнее, чем молекулы даже наилучших органических красителей. Благодаря этому те места, где собираются наночастицы золота или серебра, интенсивно окрашиваются и сразу же становятся заметными.
Другим ценным свойством НЧ золота и серебра является то, что они допускают целенаправленную модификацию своей внешней поверхности. С целью построения сенсоров, использующих свойство молекулярного распознавания, поверхность НЧ сначала химически "пассивируют", высаживая на нее тонкий слой гидрогеля. Это – короткие (до 10-20 атомов углерода в цепи) линейные полимерные молекулы (тиолы, дисульфиды, тиоэфиры), которые легко образуют прочные ковалентные связи с золотом и серебром. В растворе такие молекулы быстро присоединяются к поверхности наночастиц, формируя самоупорядоченный мономолекулярный слой (англ. selfassembled monolayers – SAM) с довольно плотной упаковкой ( рис. 3.18). С молекулами воды этот слой образует гидрогель, который надежно защищает поверхность металла от взаимодействия с другими молекулами. Потом на эту тонкую пленку гидрогеля химически высаживают молекулы-распознаватели.
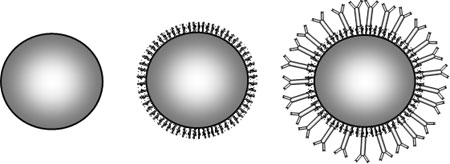
Рис. 3.18. Последовательные этапы "специализации" наночастицы металла: слева – очищенная наночастица; в центре – наночастица после пассивации; справа – после высаживания молекул-распознавателей
Подготовленные таким образом НЧ металла называют "селективными", а если молекулы-распознаватели имеют биологическое происхождение, то "биоселективными".
Биоселективные НЧ уже несколько десятилетий используют в т.н. иммунохроматографическом анализе. На рис. 3.19 показано устройство иммунохроматографической тестовой полоски, используемой при таком анализе.
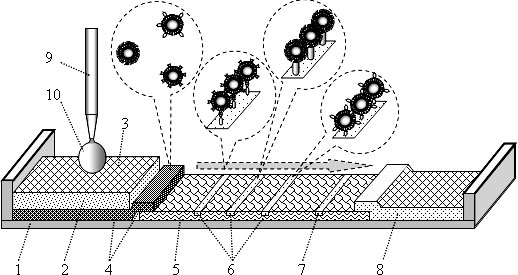
Рис. 3.19. Устройство иммунохроматографической тестовой полоски: 1 – пластмассовая основа; 2 – фильтр; 3 – приемная зона; 4 – гель с биоселективными наночастицами; 5 – хроматографическая мембрана; 6 –тестовые зоны; 7 – контрольная зона; 8 – зона абсорбции; 9 – бюретка; 10 – капля жидкой пробы
На пластмассовой основе 1 размещен фильтр 2 с приемочной зоной 3, под ними – прокладка, пропитанная гелем 4 с биоселективными НЧ. Здесь могут быть НЧ одного сорта, рассчитанные на распознавание одного аналита, или биоселективные НЧ двух-трех сортов (каждая рассчитана на свой аналит). Прокладка 4 контактирует с хроматографической мембраной 5, изготовленной чаще всего из нитроцеллюлозы. Вдоль этой мембраны капля жидкости может просачиваться, распространяясь как в хроматографической колонке. В некоторых местах мембрану пронизывают поперечные нити 6, на которые иммобилизованы антитела к соответствующему аналиту. Эти места называют тестовыми зонами или зонами сцепления. Число тестовых зон (1-3) равно числу одновременно контролируемых аналитов. В контрольной зоне 7 иммобилизованы антитела ко всем биоселективным наночастицам, особенно к тем, к которым аналит не присоединился. А в конце мембраны 5 находится абсорбционная зона 8.
Функционирование тестовой полоски объясним на примере трехкомпонентного кардиотеста "ИммунТех" производства фирмы YD Diagnostics, Южная Корея. На рис. 3.20 показан их внешний вид. На пластмассовой крышке рядом с контрольной зоной и с тестовыми зонами нанесены соответствующие сокращенные надписи, расшифрованные на рисунке справа. Над приемной зоной сформирована лунка, рядом с которой имеется тисненая надпись "S" (англ. Sample). Над зоной абсорбции имеется много отверстий, обеспечивающих свободное испарение жидкости.
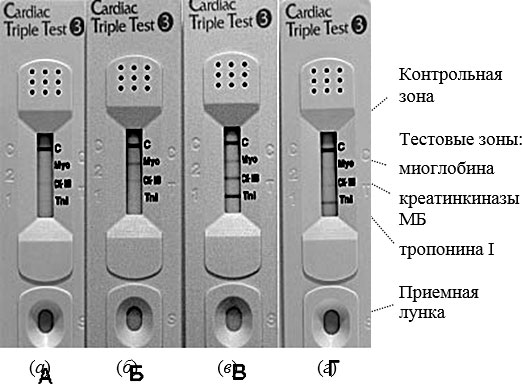
Рис. 3.20. Вид иммунохроматографической тест-полоски "Cardiac Triple Test": а) в случае, если соответствующие биомаркеры не выявлены; б) если в крови пациента имеются миоглобин и небольшое количество креатиназы; в) при типичном инфаркте миокарда; г) спустя 4-5 дней после инфаркта миокарда
В сенсоре применяются биоселективные НЧ золота трех сортов. На поверхности этих НЧ иммобилизованы молекулы, которые селективно распознают:
тропонин І (будем называть их биоселективными НЧ 1-го сорта);
креатинкиназу МБ (будем называть их биоселективными НЧ 2-го сорта);
миоглобин (будем называть их биоселективными НЧ 3-го сорта).
Молекулы всех этих трех веществ называют "кардиомаркерами", поскольку их появление в крови пациента свидетельствует о специфических изменениях в тканях его сердца.
В тестовых зонах иммобилизованы антитела, имеющие большое химическое сродство с одним из вышеназванных веществ (антитела 1-го, 2-го и 3-го сорта соответственно). Когда в приемную лунку капают пару капель крови пациента, то жидкая часть (плазма) этой крови просачивается сквозь фильтр 2 (здесь и дальше в этом абзаце см. рис. 3.19) и попадает в прокладку 4. Здесь плазма крови начинает взаимодействовать с биоселективными НЧ золота. Если в плазме крови присутствуют молекулы миоглобина, то они присоединяются к биоселективным НЧ 1-го сорта. Если присутствуют молекулы креатинкиназы МБ, то они присоединяются к биоселективным НЧ 2-го сорта. А если присутствуют молекулы тропонина І, то они присоединяются к биоселективным НЧ 3-го сорта. Левая сноска условно показывает НЧ трех сортов с присоединенными к ним молекулами аналита. Дальше подвижная жидкая фаза под действием капиллярных сил начинает просачиваться и перемещаться вдоль хроматографической мембраны 3. Направление перемещения показано на рис. 3.19 серой стрелкой. Когда подвижная жидкая фаза доходит до первой тестовой зоны 6, биоселективные НЧ 1-го сорта "захватываются" иммобилизованными здесь антителами 1-го сорта. И если молекул тропонина І в пробе крови много, то первая тестовая зона окрашивается в красный цвет, характерный для наночастиц золота. Подвижная жидкая фаза продолжает между тем перемещаться дальше. Когда она доходит до второй тестовой зоны, то иммобилизованные здесь антитела 2-го сорта захватывают биоселективные НЧ 2-го сорта, к которым присоединилась креатинкиназа МБ. И если молекул креатинкиназы в пробе крови много, то и вторая тестовая зона окрашивается в красный цвет. Когда подвижная жидкая фаза доходит до третьей тестовой зоны, то иммобилизованные здесь антитела 3-го сорта захватывают биоселективные НЧ 3-го сорта, к которым присоединилась молекула миоглобина. И если молекул миоглобина в пробе крови много, то и третья тестовая зона окрашивается в красный цвет. Дальше подвижная жидкая фаза доходит до контрольной зоны 7, где иммобилизованные здесь антитела захватывают все НЧ золота, не захваченные раньше. И контрольная зона окрашивается в красный цвет. Дальше подвижная жидкая фаза доходит до зоны абсорбции 8, из которой может свободно испаряться.
Таким образом, контрольная зона после хроматографии окрашивается практически всегда, а тестовые зоны окрашиваются в зависимости от присутствия в пробе крови соответствующих кардиомаркеров.
На рис. 3.20 показаны 4 типичных случая. В случае (а) наблюдается интенсивная окраска лишь в контрольной зоне С. Поскольку ни один из кардиомаркеров не выявлен, ни инфаркта, ни угрозы инфаркта нет. В случае (б) выявлено наличие в пробе крови миоглобина и небольшого количества креатинкиназы МБ. Это указывает врачу-кардиологу на то, что риск инфаркта миокарда у пациента довольно высок. В случае (в) наблюдается характерная картина инфаркта миокарда: присутствуют все три кардиомаркера, особенно много тропонина І. В случае (г) окрашена тестовая зона тропонина и намного слабее зона креатинина. Для врача-кардиолога – это свидетельство о том, что инфаркт миокарда произошел, причем свыше 4 суток тому назад.
Таким образом, контрольная зона после хроматографии окрашивается практически всегда, а тестовые зоны окрашиваются в зависимости от присутствия в пробе крови соответствующих кардиомаркеров.
Применение таких иммунохроматографических тестов бригадами скорой помощи, в поликлиниках, домашними врачами позволяет во много раз снизить количество диагностических ошибок, спасти много жизней и своевременно предоставить пациентам квалифицированную медпомощь.
Уже разработаны и применяются иммунохроматографические тесты для выявления свыше 150 видов заболеваний, для оценки наличия в крови человека широкой гаммы гормонов, антител, ферментов, наркотических веществ. Поскольку для анализа нужна лишь кровь, то анализ можно выполнить анонимно. Можно провести его дома или даже в дороге.